







Study with the several resources on Docsity

Earn points by helping other students or get them with a premium plan


Prepare for your exams
Study with the several resources on Docsity

Earn points to download
Earn points by helping other students or get them with a premium plan
Community
Ask the community for help and clear up your study doubts
Discover the best universities in your country according to Docsity users
Free resources
Download our free guides on studying techniques, anxiety management strategies, and thesis advice from Docsity tutors
Cours Thermodynamique S1 SMP1 2012-2013 Cours de Thermodynamique, Introduction, Description d’un syst`eme macroscopique, variables d’ ́etat, Energie, travail, chaleur, premier principe, Le gaz parfait, M ́ethodes de v ́erification des calculs, Le second principe, L’entropie, Syst`emes purs, Les autres potentiels thermodynamiques, Transitions de phase, R ́eactions chimiques, Annexes
Typology: Study Guides, Projects, Research
1 / 10

This page cannot be seen from the preview
Don't miss anything!
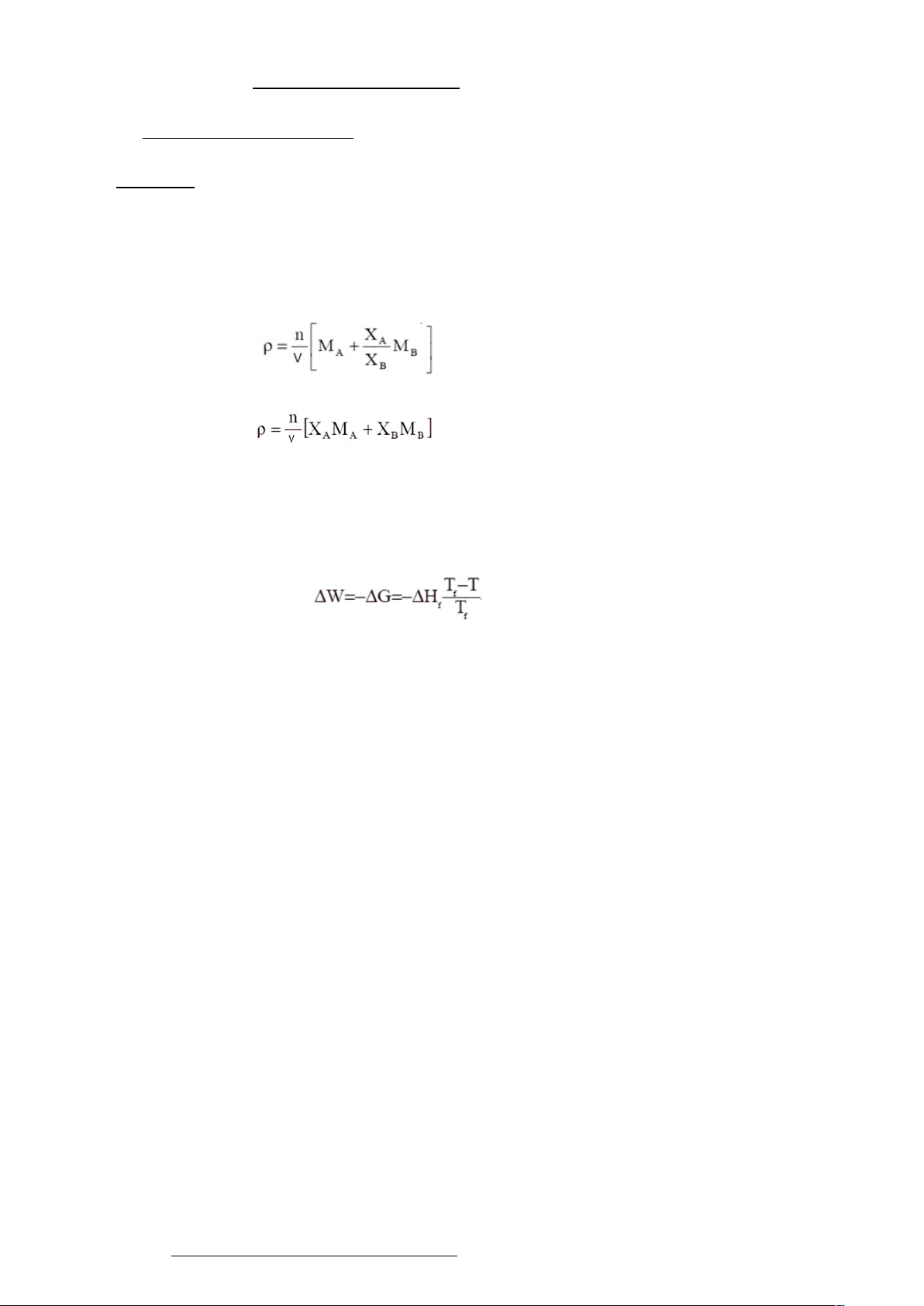






I- Recherche bibligraphique : ( Questions communes à tous les groupes) Questions : 1- On considère un alliage formé de deux elements A et B dont les fractions molaires respectives sont XA ( Solvant) et XB (Soluté). Montrer que la masse volumique « » de l’alliage peut se mettre sous l’une des deux formes suivantes en fonction de sa structure cristalline :
Sujet 1 : Alliages d’Aluminium : 1- Decrire en quelques lignes, les principaux alliages d’aluminium en précisant :
Sujet 4 : Alliages Cu-Zn : a- Quelles sont les utilisations principales des alliages Cu-Zn et donner au moins deux nuances les plus recontrées dans l’industrie. b- Quelle est la solubilité maximale du Zn dans le cuivre et que se passe-t-il au-delà de cette composition. Justifier votre réponse en précisant les avantages et les inconvenients rencontrés dans de tels alliages. Sur la figure ci-jointe, on donne le diagramme de phases du système cuivre-zinc. c- Sur ce diagramme, noter les domaines monophasés et biphasés ainsi que les différents points invariants en précisant les températures correspondantes et le type de la transformation ayant eu lieu. d- Les deux laitons commerciaux les plus communs sont
Sujet 5 :Sn-Au : Sur la figure ci-dessous, on donne le diagramme d’équilibre Etain–Or (Sn–Au). a- Dans quelles domaines on a recours aux alliages Sn-Au et donner au moins deux nuances les plus utilisées. b- Compléter les domaines du diagramme Sn-Au donné c- Quelles sont les solubilités maximales de Sn dans Au et Au dans Sn? d- Identifier les différents points invariants sur ce diagramme en prédisant les températures et la nature de la transformation correspondantes. e- Sur ce diagramme, précisez la nature et les compositions des constituants définis par les verticales notée , , , et ’: f- Un alliage composé de 40%at Sn est porté à 450°C puis refroidit lentement jusqu’à la température ambiante. Donner sa courbe de refroidissement en donnant le pourcentage et la composition massique des phases aux températures de : 300°C, 200°C et 20°C
Sujet 7 : Alliage Fe-C On considère un acier à 0.35%C et à 99.65%Fe à l’état recuit. Une coupe du diagramme Fe- C est donnée sur la figure ci-contre. a- Quelles sont les utilisations principales de ce type d’acier et indiguer ses propriétés mécaniques à son état recuit. b- Déterminer les fractions des phases suivantes présentes à l’ambiante :: i. La fraction de la ferrite et de la cémentite totales ii. La fraction de la ferrite pro-eutectoïde et de la perlite iii. La fraction de la ferrite présente dans la perlite. c- Un échantillon de cet acier oa été austénitisé à une température de 900°C pendant 30mn puis refroidis très lentement jusqu’à l’ambiante. Donner sa courbe de refroidissement et préciser sa structure finale à l’ambiante d- En chauffant cet acier à une température d’environ 800°C puis refroidi à l’air, comment evoluera sa structure metallurgique et quelles conséquences aura-t-on sur ses proriétés mécaniques. Justifier votre réponse à l’aide d’un exemple industriel.
Sujet 8 : Alliage Fe-C Vous disposez d’un acier (alliage « fer – carbone ») dont vous ignorez la teneur en carbone. Cependant, après avoir chauffé cet acier à 850 °C et l’avoir laissé refroidir lentement au four jusqu’à la température ambiante (20 °C), vous constatez, sur une métallographie de cet acier, qu’il contient 91,3 % de ferrite α et 8,7 % de cémentite Fe 3 C. a- A partir du diagramme Fe-C donné ci-dessous, quelle est la composition nominale C 0 (%m) en carbone de cet acier? b- À 724 °C, quelles sont les phases en présence, leur composition (en %m C) et leur fraction massique respective (en %m)? c- Quelle est la fraction massique de perlite présente dans l’acier à la température ambiante à la fin du refroidissement lent? d- Au cours de l’élaboration de ce type d’acier, le refroidissement est souvent plus rapide et on se retrouve loin des conditions d’équilibre. Expliquer en quelques lignes l’évolution des pourcentages des phases et leurs conséquences sur les propriétés mécaniques de cet acier. e- Donner le cycle de traitement thermique habituellement utilisé pour augmenter ses propriétés mécaniques.
Préparé par : Pr B. ouaki ENSMR, Rabat